Composto orgânico
Os compostos ou moléculas orgânicas são as substâncias químicas que contêm na sua estrutura Carbono e Hidrogênio, e muitas vezes com oxigênio, nitrogênio, enxofre, fósforo, boro, halogênios e outros. Não são moléculas orgânicas os carbetos, carbonatos, bicarbonatos, cianetos, óxidos de carbono, assim como o carbono grafite, diamante e o fulereno.
Glicose
- Moléculas orgânicas naturais: São as sintetizadas pelos seres vivos, denominadas biomoléculas, que são estudadas pela bioquímica.
- Moléculas orgânicas artificiais: São substâncias que não existem na natureza e têm sido fabricadas pelo homem, como os plásticos. A maioria dos compostos orgânicos puros são produzidos artificialmente.

A etimologia da palavra "orgânico" significa que procede de "organos", relacionada com a vida, em oposição ao inorgânico que teria o significado de tudo que carece de vida.
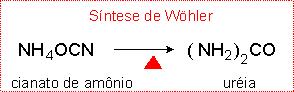
Para os químicos antigos, as substâncias orgânicas eram provenientes de fontes animais ou vegetais, e as substâncias inorgânicas seriam aquelas de procedência mineral. Durante muitos anos acreditava-se que entre a química orgânica e a química inorgância existia uma barreira intransponível. No princípio do século XIX, o químico alemão Friedrich A. Wöhler conseguiu sintetizar a uréia, um produto orgânico, a partir de substâncias inorgânicas (o cianato de amônio), comprovando que tal divisão era totalmente artificial, algo que é completamente evidente na química moderna.
Proteínas
Ligação peptídica
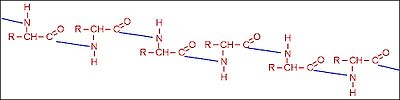
Uma ligação peptídica é uma ligação química que ocorre entre duas moléculas quando o grupo carboxilo de uma molécula reage com o grupo amina de outra molécula, liberando uma molécula de água ( H2O ). Isto é uma reação de síntese por desidratação que ocorre entre moléculas de aminoácidos.
A ligação covalente C-N resultante é chamada ligação peptídica e a grupo funcional resultante é uma amida . Polipeptídeos e proteínas são cadeias de aminoácidos presas por ligações peptídicas. A espinha dorsal do PNA ( quimicamente similar ao DNA e RNA) também é mantido por este tipo de ligação.
A ligação C-N tem um caráter parcial de dupla ligação, com o átomo de N alcançando uma carga positiva parcial e o O uma carga negativa parcial, não permitindo que a molécula normalmente gire sobre esta ligação. O arranjo inteiro dos quatro átomos C,O,N,H da ligação peptídica assim como os dois carbonos vicinais da ligação é uma estrutura planar. Esta ordenação planar rígida é o resultado da estabilização por ressonância da ligação peptídica. Por isso, o esqueleto resultante é uma série de planos sucessivos separados por grupos metilenos substituidos. Isso impõem restrições importantes no número de conformações que uma proteína pode adotar. O Nitrogenio faz apenas 3 ligaçoes covalentes , mas carrega uma molecula de hidrogenio parcialmente , sendo desprotonado na ligaçao pepitidica , formando com a hidroxila a molecula de H2O
Uma ligação peptídica pode ser quebrada por hidrólise ( adição de água ). Em determinadas condições e na presença de água, ocorre a quebra destas ligações espontaneamente com libertação de aproximadamente 10 Kj/mol de energia livre, porém o processo é extremamente lento. Em organismos vivos, o processo é facilitado pelas enzimas. Os organismos vivos também empregam enzimas para formar os peptídeos; este processo requer energia. O comprimento de onda de absorção para uma ligação peptídica é de 220-280 nm.
Aminoácido
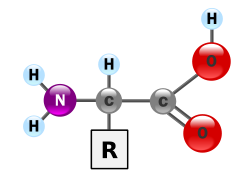 Um aminoácido é uma molécula orgânica que contém um grupo amina e um grupo carboxila, e uma cadeia lateral que é específica para cada aminoácido. Alguns aminoácidos também podem conter enxofre. Os elementos-chave de um aminoácido são carbono, hidrogênio, oxigênio e nitrogênio. Eles são particularmente importantes em bioquímica, onde o termo geralmente refere-se a alfa-aminoácidos.
São moléculas anfibólicas, ou seja, podem se comportar como ácido ou
como base liberando nesta ordem H ou OH em uma reação. Se a reação for
entre dois aminoácidos o grupo amina de um libera um H se ligando ao
grupo carboxila do outro que libera um OH formando uma peptídeo mais
H2O.
Um aminoácido é uma molécula orgânica que contém um grupo amina e um grupo carboxila, e uma cadeia lateral que é específica para cada aminoácido. Alguns aminoácidos também podem conter enxofre. Os elementos-chave de um aminoácido são carbono, hidrogênio, oxigênio e nitrogênio. Eles são particularmente importantes em bioquímica, onde o termo geralmente refere-se a alfa-aminoácidos.
São moléculas anfibólicas, ou seja, podem se comportar como ácido ou
como base liberando nesta ordem H ou OH em uma reação. Se a reação for
entre dois aminoácidos o grupo amina de um libera um H se ligando ao
grupo carboxila do outro que libera um OH formando uma peptídeo mais
H2O.A forma mais importante dos aminoácidos, os alfa-aminoácidos, que formam as proteínas, tem, geralmente, como estrutura um carbono central (carbono alfa, quase sempre quiral) ao qual se ligam quatro grupos: o grupo amina (NH2), grupo carboxílico (COOH), hidrogênio e um substituinte característico de cada aminoácido.
Os aminoácidos se unem através de ligações peptídicas, formando os peptídeos e as proteínas. Para que as células possam produzir suas proteínas, elas precisam de aminoácidos, que podem ser obtidos a partir da alimentação ou serem fabricados pelo próprio organismo.
Os aminoácidos podem ser classificados nutricionalmente, quanto ao radical e quanto ao seu destino.
Aminoácidos não-essenciais
Aminoácidos não-essenciais ou dispensáveis são aqueles que o corpo humano pode sintetizar.São eles:alanina, asparagina, ácido aspártico, ácido glutâmico, serina.
Aminoácidos essenciais
Os aminoácidos essenciais são aqueles que não podem ser produzidos pelo corpo humano. Dessa forma, são somente adquiridos pela ingestão de alimentos, vegetais ou animais.São eles: fenilalanina, isoleucina, leucina, lisina, metionina, treonina, triptofano, histidina e valina.
Aminoácidos essenciais apenas em determinadas situações fisiológicas
Aminoácidos condicionalmente essenciais são os aminoácidos que devido a determinadas patologias, não podem ser sintetizados pelo corpo humano. Assim, é necessário obter estes aminoácidos através da alimentação, de forma a satisfazer as necessidades metabólicas do organismo.São eles: arginina, cisteína, glicina, glutamina, prolina, tirosina.
Classificação quanto ao substituinte
A classificação quanto ao substituinte pode ser feita em:Aminoácidos apolares: Apresentam como substituintes hidrocarbonetos apolares ou hidrocarbonetos modificados, exceto a glicina. São substituintes hidrofóbicos.
Alanina: CH3- CH (NH2) - COOH
Leucina: CH3(CH2)3-CH2-CH (NH2)- COOH
Valina: CH3-CH(CH3)-CH (NH2)- COOH
Isoleucina: CH3-CH2-CH (CH3)-CH (NH2)- COOH
Prolina:-CH2-CH2-CH2- ligando o grupo amino ao carbono alfa
Fenilalanina: C6H5-CH2-CH (NH2)- COOH
Triptofano: R aromático- CH (NH2)- COOH
Metionina: CH3-S-CH2-CH2- CH (NH2)- COOH
Aminoácidos polares neutros: Apresentam substituintes que tendem a formar ligação de hidrogênio. Glicina: H- CH (NH2) - COOH
Serina: OH-CH2- CH (NH2)- COOH
Treonina: OH-CH (CH3)- CH (NH2)- COOH
Cisteina: SH-CH2- CH (NH2)- COOH
Tirosina: OH-C6H4-CH2- CH (NH2)- COOH
Asparagina: NH2-CO-CH2- CH (NH2)- COOH
Glutamina: NH2-CO-CH2-CH2- CH (NH2)- COOH
Aminoácidos ácidos: Apresentam substituintes com grupo carboxílico.São hidrófilos.
Ácido aspártico: HCOO-CH2- CH (NH2)- COOH
Ácido glutâmico: HCOO-CH2-CH2- CH (NH2)- COOH
Aminoácidos básicos: Apresentam substituintes com o grupo amino.
São hidrófilos Arginina: {{{1}}}- CH (NH2)- COOH
Lisina: NH3-CH2-CH2-CH2-CH2- CH (NH3)- COOH
Histidina: H-(C3H2N2)-CH2- CH (NH2)- COOH
Aminoácidos alfa
Fórmula geral
São aqueles que apresentam fórmula geral:R - CH (NH2)- COOH na qual R é uma cadeia orgânica.
No aminoácido glicina o substituinte é o hidrogênio;
O carbono ligado ao substituinte R é denominado carbono 2 ou alfa.
Os vários alfa-aminoácidos diferem em qual cadeia lateral (grupo- R) está ligado o seu carbono alfa, e podem variar em tamanho a partir de apenas um átomo de hidrogénio na glicina a um grupo heterocíclico grande como no caso do triptofano.
Outros aminoácidos encontrados na natureza
Ornitina e citrulina são α-aminoácidos que desempenham um papel vital no corpo. Eles são usados como parte do ciclo da uréia para se livrar dos iões de amónio, que de outro modo iriam nos envenenar. No entanto, não são utilizados como blocos de construção na síntese de polipéptidos.
Ácido desoxirribonucleico (DNA)
 O ácido desoxirribonucleico (ADN, em português: ácido
O ácido desoxirribonucleico (ADN, em português: ácido desoxirribonucleico; ou DNA, em inglês: deoxyribonucleic acid) é um composto orgânico cujas moléculas contêm as instruções genéticas que coordenam o desenvolvimento e funcionamento de todos os seres vivos e alguns vírus. O seu principal papel é armazenar as informações necessárias para a construção das proteínas e ARNs. Os segmentos de ADN que contêm a informação genética são denominados genes. O restante da sequência de ADN tem importância estrutural ou está envolvido na regulação do uso da informação genética.
A estrutura da molécula de ADN foi descoberta conjuntamente pelo norte-americano James Watson e pelo britânico Francis Crick em 7 de Março de 1953, o que lhes valeu o Prêmio Nobel de Fisiologia/Medicina em 1962, juntamente com Maurice Wilkins.
Do ponto de vista químico, o ADN é um longo polímero de unidades simples (monômeros) de nucleotídeos, cuja cadeia principal é formada por moléculas de açúcares e fosfato intercalados unidos por ligações fosfodiéster. Ligada à molécula de açúcar está uma de quatro bases nitrogenadas. A sequência de bases ao longo da molécula de ADN constitui a informação genética. A leitura destas sequências é feita através do código genético, que especifica a sequência linear dos aminoácidos das proteínas. A tradução é feita por um RNA mensageiro que copia parte da cadeia de ADN por um processo chamado transcrição e posteriormente a informação contida neste é "traduzida" em proteínas pela tradução. Embora a maioria do ARN produzido seja usado na síntese de proteínas, algum ARN tem função estrutural, como por exemplo o ARN ribossômico, que faz parte da constituição dos ribossomos.
Dentro da célula, o ADN pode ser observado numa estrutura chamada cromossoma durante a metáfase. O conjunto de cromossomas de uma célula forma o cariótipo. Antes da divisão celular os cromossomas são duplicados através de um processo chamado replicação. Eucariontes como animais, plantas e fungos têm o seu ADN dentro do núcleo enquanto que procariontes como as bactérias o têm disperso no citoplasma. Dentro dos cromossomas, proteínas da cromatina como as histonas compactam e organizam o ADN. Estas estruturas compactas guiam as interacções entre o ADN e outras proteínas, ajudando a controlar que partes do ADN são transcritas.
O ADN é responsável pela transmissão das características hereditárias de cada ser vivo.
Ácido ribonucleico (RNA)
O RNA é constituído por uma ribose, por um grupo fosfato e uma base nitrogenada.
A composição do RNA é muito semelhante ao do DNA (ácido desoxirribonucleico) contudo apresenta algumas diferenças:
Exemplificação de fórmula estrutural de molécula de RNA
- O RNA é formado por uma cadeia simples de nucleotídeos, e não uma de dupla hélice como o DNA. Um filamento de RNA pode se dobrar de tal modo que parte de sua próprias bases se pareiam umas com as outras. Tal pareamento intramolecular de bases é um determinante importante da forma do RNA. Assim, formando pontes intracadeia o RNA é capaz de assumir uma variedade muito maior de formas moleculares tridimensionais complexas do que a dupla hélice de DNA .
- O RNA tem o açúcar ribose em seus nucleotídeos em vez da desoxirribose encontrada no DNA. Como os nomes sugerem, os dois açúcares diferem na presença ou ausência de apenas um átomo de oxigênio. Os grupos de açúcar do RNA contêm um par oxigênio-hidrogênio ligado ao carbono 2', enquanto apenas um átomo de hidrogênio é ligado ao carbono 2' nos grupos de açúcar do DNA.
- Como um filamento individual de DNA, um filamento de RNA é formado de um arcabouço de açúcar-fosfato com uma base ligada covalentemente na posição 1' de cada ribose. As ligações açúcar-fosfato são feitas nas posições 5' e 3' do açúcar, como no DNA. Assim, uma cadeia de RNA terá uma ponta 5' e uma ponta 3'.
- Os nucleotídeos de RNA (chamados ribonucleotídeos) contêm as bases adenina (A), guanina (G), citosina (C) e uracila (U), mas esta última pirimidina, está presente em lugar de timina.
- O RNA, como a proteína mas não como DNA, pode catalisar importantes reações biológicas. As moléculas de RNA que funcionam como proteínas enzimáticas são chamadas de ribozimas.













 Posted in:
Posted in: 



